Суббота, 20.04.2024, 11:52
ХИМБИО-INFORM: Сайт учителя химии и биологии Ващенко Н.Ю.
|
Меню сайта
Погода в Ногинске
Живой календарь
Мини-чат
Новости
|
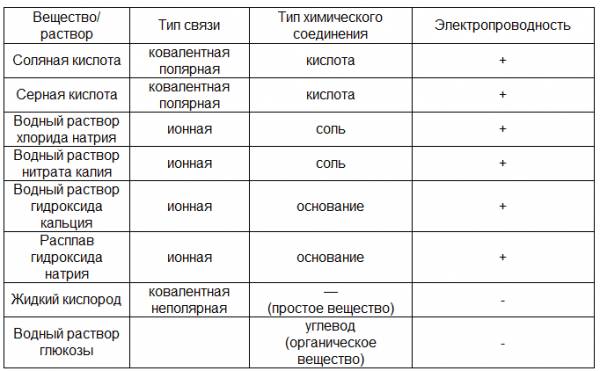
Электролиты и неэлектролиты. Электролитическая диссоциация веществ в водных растворахТЕОРИЯ ЭЛЕКТРОЛИТИЧЕСКОЙ ДИССОЦИАЦИИ Растворы всех веществ можно разделить на две группы: проводят электрический ток или проводниками не являются. С особенностями растворения веществ можно познакомиться экспериментально, исследуя электропроводность растворов этих веществ с помощью прибора, изображённого на рисунке  Пронаблюдайте за следующим экспериментом «Изучение электрической проводимости веществ». Для объяснения особенностей водных растворов электролитов шведским ученым С. Аррениусом в 1887 г. была предложена теория электролитической диссоциации. В дальнейшем она была развита многими учеными на основе учения о строении атомов и химической связи. Современное содержание этой теории можно свести к следующим трем положениям: 1. Электролиты при растворении в воде или расплавлении распадаются (диссоциируют) на ионы – положительно (катионы) и отрицательно (анионы) заряженные частицы. Ионы находятся в более устойчивых электронных состояниях, чем атомы. Они могут состоять из одного атома - это простые ионы (Na+, Mg2+, Аl3+ и т.д.) - или из нескольких атомов - это сложные ионы (NО3-, SO2-4, РОЗ-4 и т.д.). 2. В растворах и расплавах электролиты проводят электрический ток. Под действием электрического тока ионы приобретают направленное движение: положительно заряженные ионы движутся к катоду, отрицательно заряженные - к аноду. Поэтому первые называются катионами, вторые - анионами. Направленное движение ионов происходит в результате притяжения их противоположно заряженными электродами.
ЭЛЕКТРОЛИТЫ И НЕЭЛЕКТРОЛИТЫ
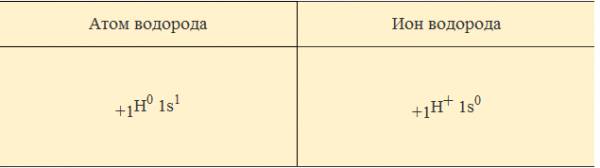
 3. Диссоциация - обратимый процесс: параллельно с распадом молекул на ионы (диссоциация) протекает процесс соединения ионов (ассоциация). Поэтому в уравнениях электролитической диссоциации вместо знака равенства ставят знак обратимости. Например, уравнение диссоциации молекулы электролита КA на катион К+ и анион А- в общем виде записывается так: КА ↔ K+ + A- Интерактивное объяснение материала по теме Рассмотрим процесс растворения электролитов в воде В целом молекула воды не заряжена. Но внутри молекулы Н2О атомы водорода и кислорода располагаются так, что положительные и отрицательные заряды находятся в противоположных концах молекулы (рис. 1). Поэтому молекула воды представляет собой диполь.  Рис. 1. Молекула воды полярна и представляет собой диполь Растворение в воде веществ с ионной химической связью (на примере хлорида натрия – поваренной соли) Механизм электролитической диссоциации NaCl при растворении поваренной соли в воде (рис. 2) состоит в последовательном отщеплении ионов натрия и хлора полярными молекулами воды. Вслед за переходом ионов Na+ и Сl– из кристалла в раствор происходит образование гидратов этих ионов.  Рис. 2. Механизм растворения хлорида натрия в воде: а – ориентация молекул воды на поверхности кристалла NaCl и отрыв иона Na+; б – гидратация (окружение молекулами воды) ионов Na+ и Сl– Растворение в воде веществ с ковалентной сильнополярной химической связью (на примере соляной кислоты) При растворении в воде соляной кислоты (в молекулах HCl cвязь между атомами ковалентная сильнополярная) происходит изменение характера химической связи. Под влиянием полярных молекул воды ковалентная полярная связь превращается в ионную. Образовавшиеся ионы остаются связанными с молекулами воды – гидратированными. Если растворитель неводный, то ионы называют сольватированными (рис.3).  Рис. 3. Диссоциация молекул HCl на ионы в водном растворе Основные положения: Электролитическая диссоциация – это процесс распада электролита на ионы при растворении его в воде или расплавлении. Электролиты – это вещества, которые при растворении в воде или в расплавленном состоянии распадаются на ионы. Ионы – это атомы или группы атомов, обладающие положительным (катионы) или отрицательным (анионы) зарядом. Ионы отличаются от атомов как по строению, так и по свойствам Пример 1. Сравним свойства молекулярного водорода (состоит из двух нейтральных атомов водорода) со свойствами иона. Посмотрите опыт. Пример 2. Сравним свойства атомарного и молекулярного хлора со свойствами иона. Запомните! 1. Ионы отличаются от атомов и молекул по строению и свойствам; 2. Общий и характерный признак ионов – наличие электрических зарядов; 3. Растворы и расплавы электролитов проводят электрический ток из-за наличия в них ионов. Тренажёр "Определение электрической проводимости растворов веществ" Тренажёр "Электролиты и неэлектролиты" |
Новости сайта
Поздравляем победителей и лауреатов Всероссийских дистанционных олимпиад по химии и биологии Наш опрос
Представьтесь, Вы...
Всего ответов: 184
Полезные ссылки
    
 
 Друзья сайта
Архив записей
|
|