Философская истина: все в нашем мире относительно, – справедлива и для классификации веществ и их свойств. Великое многообразие веществ во Вселеннойи на нашей планете состоит всего лишь из 90 химических элементов. В природе встречаются вещества, построенные элементами с порядковыми номерами с 1 по 91 включительно. Элемент 43 – технеций, в настоящее время на Земле в природе не обнаружен, т.к. этот элемент не имеет стабильных изотопов. Он был получен искусственно в результате ядерной реакции. Отсюда и название элемента – от греч. téhnos – искусственный.
Все земные природные химические вещества, построенные из 90 элементов, можно разделить на два больших типа – неорганические и органические.
Органическими веществами называют соединения углерода за исключением простейших: оксидов углерода, карбидов металлов, угольной кислоты и ее солей. Все остальные вещества относятся к неорганическим.
Органических веществ насчитывается более 27 млн – гораздо больше, чем неорганических, число которых по самым оптимистическим подсчетам не превышает 400 тыс. О причинах многообразия органических соединений мы поговорим чуть позже, а пока отметим, что резкой границы между двумя этими группами веществ не существует. Например, соль изоцианат аммония NH4NCO считается неорганическим соединением, а мочевина (NH2)2CO, имеющая точно такой же элементный состав N2H4CO, – вещество органическое.
Вещества, имеющие одинаковую молекулярную формулу, но разное химическое строение, называются изомерами.
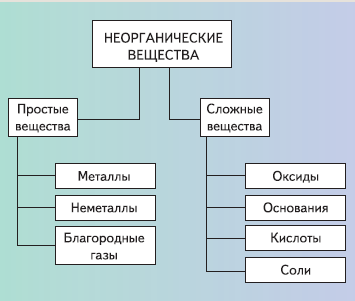
Неорганические вещества принято делить на два подтипа – простые и сложные (схема 1). Как вы уже знаете, простыми называют вещества, состоящие из атомов одного химического элемента, а сложные – из двух и более химических элементов.
Схема 1
Все земные природные химические вещества, построенные из 90 элементов, можно разделить на два больших типа – неорганические и органические.
Органическими веществами называют соединения углерода за исключением простейших: оксидов углерода, карбидов металлов, угольной кислоты и ее солей. Все остальные вещества относятся к неорганическим.
Органических веществ насчитывается более 27 млн – гораздо больше, чем неорганических, число которых по самым оптимистическим подсчетам не превышает 400 тыс. О причинах многообразия органических соединений мы поговорим чуть позже, а пока отметим, что резкой границы между двумя этими группами веществ не существует. Например, соль изоцианат аммония NH4NCO считается неорганическим соединением, а мочевина (NH2)2CO, имеющая точно такой же элементный состав N2H4CO, – вещество органическое.
Вещества, имеющие одинаковую молекулярную формулу, но разное химическое строение, называются изомерами.
Неорганические вещества принято делить на два подтипа – простые и сложные (схема 1). Как вы уже знаете, простыми называют вещества, состоящие из атомов одного химического элемента, а сложные – из двух и более химических элементов.
Схема 1
Классификация неорганических веществ
Казалось бы, число простых веществ должно совпадать с числом химических элементов. Однако это не так. Дело в том, что атомы одного и того же химического элемента могут образовывать не одно, а несколько различных простых веществ. Такое явление, как вы знаете, называют аллотропией. Причинами аллотропии может быть разное число атомов в молекуле (например, аллотропные модификации элемента кислорода – кислород О2 и озон О3), а также различное строение кристаллической решетки твердого вещества (например, уже знакомые вам аллотропные видоизменения углерода – алмаз и графит).
В подтипе простых веществ выделяют металлы, неметаллы и благородные газы, причем последние часто относят к неметаллам. В основе такой классификации лежат свойства простых веществ, обусловленные строением атомов химических элементов, из которых эти вещества образованы, и типом кристаллической решетки. Всем известно, что металлы проводят электрический ток, теплопроводны, пластичны, обладают металлическим блеском. Неметаллы, как правило, такими свойствами не обладают. Наша оговорка «как правило» не случайна, и она еще раз подчеркивает относительность классификации простых веществ. Некоторые металлы по свойствам напоминают неметаллы (например, аллотропная модификация олова – серое олово – порошок серого цвета, не проводит электрический ток, лишено блеска и пластичности, тогда как белое олово, другая аллотропная модификация, – типичный металл). Напротив, неметалл графит, аллотропная модификация углерода, весьма электропроводен и обладает характерным металлическим блеском.
Самая общая классификация сложных неорганических веществ хорошо вам знакома из курса химии основной школы. Здесь выделяют четыре класса соединений: оксиды, основания, кислоты и соли.
Деление неорганических веществ на классы проводят на основании их состава, который, в свою очередь, отражается на свойствах соединений. Напомним определения представителей каждого класса.
Оксиды – сложные вещества, состоящие из двух элементов, один из которых – кислород в степени окисления –2 (например, Н2О, СО2, CuO).
Основания – это сложные вещества, состоящие из атома металла и одной или нескольких гидроксигрупп (например, NaOH, Ca(OH)2).
Кислоты – это сложные вещества, состоящие из атомов водорода и кислотного остатка (например, HCl, HNO3, H2SO4, H3PO4).
Соли – это сложные вещества, состоящие из атомов металла и кислотных остатков (например, NaNO3, K2SO4, AlCl3).
Подобная классификация и определения также весьма относительны. Во-первых, роль металла в основаниях и солях могут выполнять сложные частицы наподобие знакомоговам катиона аммония NH4+, состоящего только из элементов неметаллов. Во-вторых, существует достаточно многочисленная группа веществ, которые пформальным признакам (по составу) являются основаниями, а по свойствам относятся к амфотерным гидроксидам, т.е. сочетают свойства оснований и кислот. Например, гидроксид алюминия Al(OH)3 при взаимодействии с кислотой ведет себя как основание:
Al(OH)3 + 3HCl = AlCl3 + 3H2O,
а при сплавлении со щелочами проявляет свойства кислоты:
H3AlO3 + NaOH = NaAlO2 + H2O.
В-третьих, в приведенную выше классификацию сложных неорганических веществ не попадает большое число соединений, которые нельзя отнести ни к одному из перечисленных классов. Это, например, соединения, образованные двумя или более элементами-неметаллами (хлорид фосфора(V) PCl5, сульфид углерода CS2, фосген COCl2).
? 1. Какие вещества называются неорганическими, а какие – органическими? Приведите примеры. Докажите относительность такой классификации веществ.
2. Какие вещества называются простыми, а какие – сложными? Почему число простых веществ превышает число химических элементов?
3. Какова классификация простых веществ? Приведите примеры веществ каждого типа. Благородные газы являются веществами атомного или молекулярного строения? Приведите аргументы в пользу той и другой точек зрения.
4. Какие неорганические вещества называются оксидами, основаниями, кислотами, солями? Приведите примеры веществ каждого класса, проиллюстрируйте их свойства двумя-тремя уравнениями химических реакций.
5. С помощью уравнений химических реакций докажите, что амфотерные гидроксиды проявляют свойства как кислот, так и оснований.
6. Карбонат кальция (мел, мрамор, известняк) вдохновлял скульпторов, художников, поэтов. Например:
В подтипе простых веществ выделяют металлы, неметаллы и благородные газы, причем последние часто относят к неметаллам. В основе такой классификации лежат свойства простых веществ, обусловленные строением атомов химических элементов, из которых эти вещества образованы, и типом кристаллической решетки. Всем известно, что металлы проводят электрический ток, теплопроводны, пластичны, обладают металлическим блеском. Неметаллы, как правило, такими свойствами не обладают. Наша оговорка «как правило» не случайна, и она еще раз подчеркивает относительность классификации простых веществ. Некоторые металлы по свойствам напоминают неметаллы (например, аллотропная модификация олова – серое олово – порошок серого цвета, не проводит электрический ток, лишено блеска и пластичности, тогда как белое олово, другая аллотропная модификация, – типичный металл). Напротив, неметалл графит, аллотропная модификация углерода, весьма электропроводен и обладает характерным металлическим блеском.
Самая общая классификация сложных неорганических веществ хорошо вам знакома из курса химии основной школы. Здесь выделяют четыре класса соединений: оксиды, основания, кислоты и соли.
Деление неорганических веществ на классы проводят на основании их состава, который, в свою очередь, отражается на свойствах соединений. Напомним определения представителей каждого класса.
Оксиды – сложные вещества, состоящие из двух элементов, один из которых – кислород в степени окисления –2 (например, Н2О, СО2, CuO).
Основания – это сложные вещества, состоящие из атома металла и одной или нескольких гидроксигрупп (например, NaOH, Ca(OH)2).
Кислоты – это сложные вещества, состоящие из атомов водорода и кислотного остатка (например, HCl, HNO3, H2SO4, H3PO4).
Соли – это сложные вещества, состоящие из атомов металла и кислотных остатков (например, NaNO3, K2SO4, AlCl3).
Подобная классификация и определения также весьма относительны. Во-первых, роль металла в основаниях и солях могут выполнять сложные частицы наподобие знакомоговам катиона аммония NH4+, состоящего только из элементов неметаллов. Во-вторых, существует достаточно многочисленная группа веществ, которые пформальным признакам (по составу) являются основаниями, а по свойствам относятся к амфотерным гидроксидам, т.е. сочетают свойства оснований и кислот. Например, гидроксид алюминия Al(OH)3 при взаимодействии с кислотой ведет себя как основание:
Al(OH)3 + 3HCl = AlCl3 + 3H2O,
а при сплавлении со щелочами проявляет свойства кислоты:
H3AlO3 + NaOH = NaAlO2 + H2O.
В-третьих, в приведенную выше классификацию сложных неорганических веществ не попадает большое число соединений, которые нельзя отнести ни к одному из перечисленных классов. Это, например, соединения, образованные двумя или более элементами-неметаллами (хлорид фосфора(V) PCl5, сульфид углерода CS2, фосген COCl2).
? 1. Какие вещества называются неорганическими, а какие – органическими? Приведите примеры. Докажите относительность такой классификации веществ.
2. Какие вещества называются простыми, а какие – сложными? Почему число простых веществ превышает число химических элементов?
3. Какова классификация простых веществ? Приведите примеры веществ каждого типа. Благородные газы являются веществами атомного или молекулярного строения? Приведите аргументы в пользу той и другой точек зрения.
4. Какие неорганические вещества называются оксидами, основаниями, кислотами, солями? Приведите примеры веществ каждого класса, проиллюстрируйте их свойства двумя-тремя уравнениями химических реакций.
5. С помощью уравнений химических реакций докажите, что амфотерные гидроксиды проявляют свойства как кислот, так и оснований.
6. Карбонат кальция (мел, мрамор, известняк) вдохновлял скульпторов, художников, поэтов. Например:
Видишь мрамор? Это просто кальций.
Химия. Породистый кристалл.
Но коснулись этой глыбы пальцы,
И Венерой вышла красота.
И.Сельвинский
Какую химическую ошибку допускает поэт в этом четверостишии?








